Tóm tắt
Nghiên cứu tính chất của nước vỉa có thể đánh giá triển vọng của dầu cũng như nhận diện các vỉa dầu và vỉa nước. Trong số các ion thành phần của nước vỉa, bromide và iodide là hai nguyên tố quan trọng phản ánh môi trường, độ khoáng hóa cũng như mức độ khép kín của vỉa chứa. Nhóm tác giả tập trung nghiên cứu xác định nồng độ bromide và iodide trong nước vỉa bằng phương pháp phân tích trắc quang UV-Vis. Đây là phương pháp đã được đề cập trong bộ tiêu chuẩn “Các phương pháp phân tích tiêu chuẩn cho nước và nước thải” được sử dụng trên thế giới nhưng lần đầu tiên được áp dụng tại Việt Nam trên đối tượng nước vỉa dầu khí. Phương pháp này cho giới hạn phát hiện thấp đến 0,1mg/L, độ tái lặp trên 10 mẫu đo cũng như độ lệch so với 10 mẫu gửi phân tích đối chứng bằng cả 2 phương pháp (phân tích đối chứng bằng phương pháp sắc kí ion đối với Br- và chuẩn độ điện thế đối với ion I-) đều nhỏ hơn 5%. Kết quả phân tích được kiểm chứng với đơn vị phân tích độc lập khác và qua đó cho phép ứng dụng rộng rãi trong phân tích nước vỉa dầu khí nói riêng và phân tích nước nói chung.
1. Nguồn gốc và ý nghĩa của bromide và iodide trong nước vỉa [1, 2]
Iodide và bromide là các nguyên tố giải phóng từ động thực vật trôi nổi và bám đáy ở vùng biển nóng và kín, khó tồn tại ở điều kiện nhiệt độ cao mà thường ở dưới dạng hợp chất với các nguyên tố khác trong đất.
Bromide thường được tìm thấy trong nước biển, rong biển và cỏ biển. Trong nước vỉa, bromide phản ánh mức độ khép kín của mỏ. Sau khi phân hủy vật liệu hữu cơ đặc biệt là rong tảo, cỏ biển, bromide tiếp tục tồn tại trong bùn ở giai đoạn tạo đá (diagenes) và sau đó tách ra khỏi bùn rồi hòa tan vào nước ngầm. Trong nước biển, bromide thường có giá trị khoảng 64mg/L.
Iodide thường được tìm thấy trong nước biển với nồng độ rất thấp (khoảng 0,05mg/L) chủ yếu do sự phân hủy từ vật liệu hữu cơ. Theo A.V.Cudelskii, iodide có nồng độ cao khi độ khoáng hóa của nước cao và tỷ lệ nghịch với nồng độ ion SO42-. Iodide có nguồn gốc từ rong tảo, cỏ biển và thường đi kèm với các nguyên tố khác như: Al, Si, Mn, P, Br.
Quá trình tích lũy, bảo tồn iodide thường đi kèm với sự hình thành của dầu khí nên việc xuất hiện iodide có thể là dấu hiệu để nhận biết dầu khí. Iodide tồn tại trong sinh vật ở dạng iodine, sau khi phân hủy vật liệu hữu cơ tạo thành iodide được tích lũy trong nước, thường dưới dạng muối hay hỗn hợp với khoáng vật, ít khi ở trạng thái tự do. Bể Trầm tích càng dày thì càng có điều kiện tích lũy nhiều nồng độ iodide [1]. Ví dụ: bể có bề dày trầm tích < 4 - 5km thì iodide thường chỉ có giá trị rất thấp (2,9mg/L đến < 10mg/L). Nếu bề dày trầm tích lớn hơn 7km thì có khả năng giàu iodide.
2. Phương pháp trắc quang xác định nồng độ bromide và iodide trong nước vỉa
2.1. Phương pháp trắc quang với chỉ thị phenol đỏ nhằm xác định bromide [3]
Khi mẫu chứa ion Br- được thêm dung dịch chloramine-T với sự có mặt của chỉ thị phenol đỏ, quá trình oxy hóa ion Br- xảy ra ngay lập tức. Nếu khống chế pH của phản ứng trong khoảng 4,5 - 4,7 thì màu của phản ứng sẽ chuyển từ đỏ cam sang ánh tím tùy thuộc vào nồng độ ion Br- trong dung dịch. Trong phương pháp này, nồng độ chloramine-T và thời gian phản ứng là hai yếu tố quan trọng giúp cho sự tạo màu và định lượng chính xác nồng độ ion Br-.
2.2. Phương pháp trắc quang với chỉ thị leuco crystal violet nhằm xác định iodide [4]
Iodide (I-) sẽ bị oxy hóa thành iodine (I2) với tác nhân oxy hóa mạnh là KHSO5. Iodine tạo thành sẽ phản ứng với thuốc thử không màu 4,4’,4”-methylidynetris (N,N- dimethylaniline) (thuốc thử leuco crystal violet) để tạo thành hợp chất màu violet đặc trưng. Phương pháp cho hợp chất phức tạo thành có sắc độ màu ổn định và tuân theo định luật hấp thụ Bugar-Lambert-Beer trong khoảng nồng độ I- tương đối lớn. Độ hấp thụ quang đo được phụ thuộc rất lớn vào giá trị pH của dung dịch đo và giá trị này phải được giữ ổn định từ 3,5 - 4,0 ở bước sóng 592nm. Việc điều chỉnh giá trị pH chính xác có ảnh hưởng lớn đến độ chính xác của phép đo, quyết định tính chính xác của phương pháp đo.
2.3. Ưu điểm, hạn chế
Phương pháp trắc quang xác định bromide sử dụng chỉ thị phenol đỏ hiện cũng được sử dụng khá phổ biến. Phương pháp cho giới hạn phát hiện thấp (khoảng 0,1mg/L, tương đương với phương pháp sắc ký ion - chi phí đầu tư trang thiết bị cao), thao tác chuẩn bị hóa chất tiền thí nghiệm cũng như các bước thí nghiệm được thực hiện đơn giản; giá thành thiết bị phân tích trắc quang tương đối thấp, có thể sử dụng thiết bị để phân tích nhiều thành phần khác nhau trong nước (anion, cation, phức chất...).
Tuy nhiên, phương pháp này có hạn chế nhất định: sự ảnh hưởng lớn từ màu dung dịch gốc và yếu tố pha loãng mẫu...
Phương pháp trắc quang xác định iodide với chỉ thị leuco crystal violet có tính ứng dụng cao với ưu điểm: chi phí đầu tư thiết bị thấp, thao tác chuẩn bị hóa chất và thực hiện thí nghiệm tương đối đơn giản. Tuy nhiên, phương pháp này cũng có hạn chế nhất định như: độ nhạy phát hiện không cao bằng các phương pháp điện thế, khử xúc tác…; yếu tố pha loãng mẫu và màu sắc của dung dịch gốc ban đầu cũng ảnh hưởng lớn đến quá trình phát triển màu khi thêm thuốc thử, từ đó ảnh hưởng đến độ chính xác của phép đo. Đây cũng chính là nguyên nhân dẫn đến việc một số mẫu nước vỉa có màu cường độ mạnh có thể sẽ không thể phân tích được bằng phương pháp này.
3. Thực nghiệm
3.1. Dụng cụ, thiết bị
- Máy trắc quang UV-Vis Cary 50, dùng đo ở bước sóng 590nm và 592nm (Hình 1).
- Dụng cụ thủy tinh sử dụng trong thí nghiệm như: cốc 100ml, bình tam giác, pipet... được rửa bằng dung dịch acid HNO3 1:6 (v/v) và tráng lại bằng nước cất để loại bỏ các tạp chất còn lưu lại.
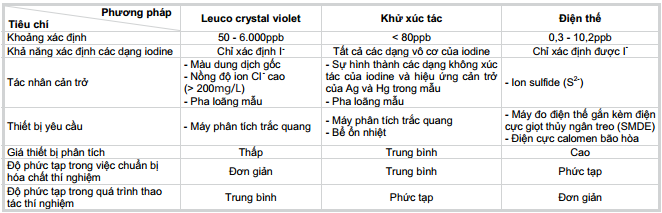
| Bảng 1. So sánh các phương pháp xác định nồng độ bromide |
 |
| |
| Bảng 2. So sánh các phương pháp xác định nồng độ iodine |
 |
 |
| Hình 1.
Hệ thống máy phân tích trắc quang UV-Vis Cary 50 kết hợp với máy tính
và bộ cuvet đo mẫu tại Phòng thí nghiệm địa hóa - Viện Dầu khí Việt Nam |
3.2. Hóa chất
- Dung dịch đệm acetate
- Dung dịch chỉ thị phenol đỏ
- Dung dịch chloramine-T
- Dung dịch sodium thiosulfate, 2M
- Dung dịch gốc Br-
- Nước cất loại I2
- Dung dịch gốc I-
- Dung dịch đệm citric pH 3,8
- Chỉ thị leuco crystal violet
- Dung dịch potassium peroxymonosulfate
3.3. Lập đường chuẩn và phân tích mẫu
3.3.1. Phương pháp xác định nồng độ bromide
Chuẩn bị tối thiểu 6 dung dịch chuẩn có nồng độ Br- tăng dần (0mg, 0,2mg, 0,4mg, 0,6mg, 0,8mg, 1mg Br-/L) nằm trong khoảng tuyến tính của đường chuẩn [3]. Trong thực tế, mẫu nước vỉa hoặc nước biển sẽ được pha loãng để nồng độ Br- rơi vào trong khoảng tuyến tính của đường chuẩn.
Cho dung dịch đệm, dung dịch chỉ thị phenol đỏ và dung dịch chloramine-T vào các mẫu dung dịch chuẩn rồi lắc đều. Sau 20 phút, cho them dung dịch Sodium thiosulfate (Na2S2O3) vào các mẫu dung dịch chuẩn, lắc đều rồi đem đo độ hấp thụ quang Am ở bước sóng 590nm với mẫu nền là nước cất được xử lý lên màu và lập đường chuẩn cùng hệ số tương quan R2.
Thực tế, sau khi lập dãy dung dịch chuẩn (Hình 2) và tiến hành đo độ hấp thụ quang ở bước song 590nm với các nồng độ khác nhau của dãy dung dịch chuẩn, thu được đồ thị và phương trình tương quan tuyến tính như sau:
 |
 |
Hình 2. Dãy dung dịch chuẩn có nồng độ Br- tăng dần từ 0 - 1mg/L
lập tại Phòng thí nghiệm địa hóa - Viện Dầu khí Việt Nam |
Biểu diễn các giá trị lên đồ thị có được đường chuẩn như Hình 3.
Hình 3 và phương trình (1) cho thấy quan hệ giữa nồng độ dung dịch Br- khảo sát (0 - 1mg Br/L) với độ hấp thụ quang có mối quan hệ tuyến tính tốt (R2 > 0,95) nên có thể sử dụng khoảng nồng độ khảo sát này để phân tích nồng độ Br- thực tế trong mẫu.
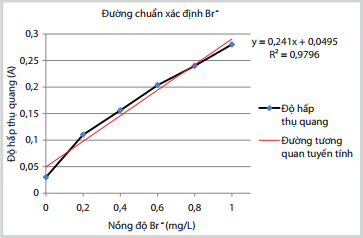 |
Hình 3. Đường chuẩn xác định Br- bằng phương pháp trắc quang
lập tại Phòng thí nghiệm địa hóa - Viện Dầu khí Việt Nam |
Phân tích mẫu thực tế bằng cách cho thêm dung dịch đệm, dung dịch chỉ thị phenol đỏ và dung dịch chloramine-T vào mẫu rồi lắc đều. Sau 20 phút, cho them dung dịch Na2S2O3 vào mẫu, lắc đều rồi đem đo độ hấp thụ quang Am ở bước sóng 590nm. Từ giá trị độ hấp thụ quang đo được, kết hợp với phương trình (1) có thể tính toán chính xác nồng độ Br- trong mẫu. Công thức tính có dạng như sau:
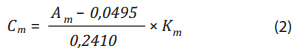 |
Trong đó:
Cm: Nồng độ Br- trong mẫu phân tích (mg/L hoặcppm);
Am: Độ hấp thụ quang của dung dịch phân tích tại bước sóng 590nm;
Km: Hệ số pha loãng mẫu. Hệ số này thay đổi tùy theo nồng độ thực tế của mẫu phân tích sao cho giá trị cuối rơi vào khoảng tuyến tính của đường chuẩn đã lập.
3.3.2. Phương pháp xác định nồng độ iodide
Chuẩn bị dãy dung dịch chuẩn có nồng độ I- tăng dần từ 0 - 6mg I-/L với mức tăng khoảng 0,5mg/L hoặc lớn hơn. Quá trình lên màu đối với từng mẫu dung dịch chuẩn được thực hiện như sau:
Cho 50ml dung dịch chuẩn vào bình định mức 100ml, cho tiếp dung dịch đệm citric và KHSO5. Lắc đều và để yên trong khoảng 1 phút. Sau đó, cho tiếp chỉ thị leuco crystal violet để dung dịch trong bình định mức đạt 100ml và lắc đều. Sau 5 phút, tiến hành đọc độ hấp thụ của dung dịch trên máy phân tích trắc quang tại bước sóng 592nm (Hình 4).
 |
Hình 4. Dãy dung dịch chuẩn có nồng độ I- tăng dần từ 0 - 6mg/L
lập tại Phòng thí nghiệm địa hóa - Viện Dầu khí Việt Nam |
Cơ chế phản ứng được mô tả như sau:
Tác nhân tạo màu chính với thuốc thử không màu leuco crystal violet trong dung dịch là iodine (I2). Sử dụng tác nhân oxy hóa mạnh như KHSO5 để oxy hóa I- thành I2.
Phương trình phản ứng dạng ion được mô tả như sau:
I2 tạo thành lập tức phản ứng với thuốc thử cho màu đặc trưng của phẩm màu crystal violet (màu tím hoa cà). Như vậy, bản chất của việc xác định nồng độ I- bằng phương pháp này chính là thông qua việc xác định nồng độ I2 tạo thành trung gian do kết quả của quá trình oxy hóa I- thành I2 với tác nhân oxy hóa KHSO5.
Trên thực tế, sau khi lập dãy dung dịch chuẩn và tiến hành đo độ hấp thụ quang ở 592nm ở các nồng độ khác nhau của dãy dung dịch chuẩn, thu được đồ thị và phương trình tương quan tuyến tính như sau:
A = 0,0833 × Cm + 0,0299 (R2 = 0,9859) (3)
Trong đó:
A: Độ hấp thụ quang của mẫu đo;
Cm: Nồng độ (mg/L hoặc ppm).
Biểu diễn các giá trị lên đồ thị có được đường chuẩn như Hình 5.
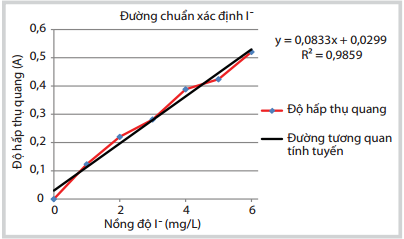 |
Hình 5. Đường chuẩn xác định I- bằng phương pháp trắc quang
lập tại Phòng thí nghiệm địa hóa - Viện Dầu khí Việt Nam |
Hình 5 và phương trình (3) cho thấy giữa nồng độ dung dịch I- trong khoảng khảo sát (0 - 6mg I-/L) và độ hấp thụ quang có mối quan hệ tuyến tính tốt (R2 > 0,95) nên có thể sử dụng khoảng nồng độ khảo sát này để phân tích nồng độ I- thực tế có trong mẫu theo phương pháp đường chuẩn tương quan tuyến tính.
Phân tích mẫu thực tế bằng cách cho 50ml mẫu dung dịch chuẩn vào bình định mức 100ml, tiến hành các bước lên màu và đọc độ hấp thụ quang Am1. Kết hợp với phương trình (2) để xác định nồng độ I- ban đầu. Trường hợp dung dịch mẫu phân tích có nồng độ I- > 6mg/L, tiến hành cho 25ml mẫu vào bình định mức 100ml rồi thực hiện các bước lên màu như bình thường. Sử dụng Bảng 3 để biết thể tích mẫu cần thiết cho việc phân tích I- ở các nồng độ khác nhau.
Bước tiếp theo, cho 50ml mẫu vào bình định mức 100ml, tiến hành các bước lên màu như trên nhưng không cho KHSO 5. Tiến hành đọc độ hấp thụ quang Am2. Từ phương trình (3) và độ hấp thụ quang đo được trên mẫu cho và không cho KHSO5 tại bước sóng 592nm tính được nồng độ I- trong dung dịch theo công thức (4):
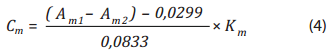 |
Cm: Nồng độ I- trong mẫu phân tích (mg/L hoặc ppm);
Am1, Am2: Độ hấp thụ quang của dung dịch phân tích khi cho và không cho KHSO5 tại bước sóng 592nm;
Km: Hệ số pha loãng mẫu. Hệ số này thay đổi tùy theo nồng độ thực tế của mẫu phân tích sao cho giá trị cuối rơi vào khoảng tuyến tính của đường chuẩn đã lập.
3.4. Đánh giá kết quả phân tích
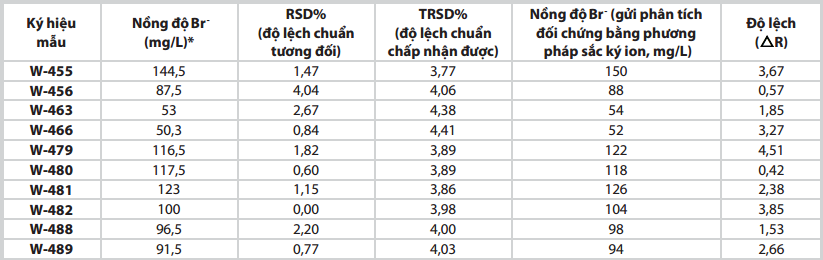
Bảng 4 thể hiện đầy đủ các thông tin về độ tái lặp cũng như độ đúng (đối chiếu với đơn vị phân tích bên ngoài ) đối với phương pháp xác định nồng độ Br- bằng phân tích trắc quang trên 10 mẫu nước vỉa tại phòng thí nghiệm. Từ đây, có thể nhận thấy độ tái lặp rất tốt đối với 10 mẫu phân
tích. Các giá trị RSD% đều thấp hơn giá trị TRSD% tương ứng. Điều này cho thấy độ ổn định của phương pháp phân tích, đồng thời khẳng định độ tái lặp của các kết quả phân tích là chấp nhận được. Độ đúng được đánh giá qua độ lệch giữa kết quả phân tích tại phòng thí nghiệm với kết quả gửi phân tích đối chứng (sử dụng phương pháp sắc kí ion đối với Br- và chuẩn độ điện thế đối với ion I-) đều nằm trong phạm vi cho phép (< 5%). Có 4 trong tổng số 10 mẫu có độ lệch rất thấp như W-456, W-463, W-480, W-488 (< 2%) phản ánh mức độ chính xác của phương pháp thử nghiệm trên các đối tượng mẫu này.
| Bảng 3. Thể tích mẫu thích hợp cho phân tích I- ở các nồng độ khác nhau |
 |
| Bảng 4. Kết quả phân tích nồng độ Br- trên 10 mẫu nước vỉa tại Phòng thí nghiệm và gửi phân tích đối chứng tại QUATEST 3 |
 |
| (*): n = 2 |
| Bảng 5. Kết quả phân tích nồng độ I- trên 10 mẫu nước vỉa tại Phòng thí nghiệm và gửi phân tích đối chứng tại QUATEST 3 |
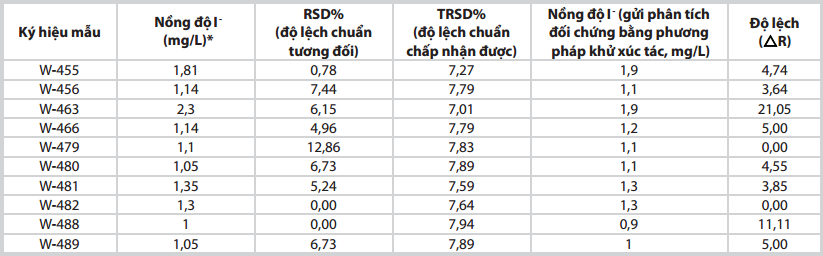 |
Bảng 5 cho thấy có 9 trong tổng số 10 mẫu đo có các giá trị RSD% thấp hơn giá trị TRSD% chấp nhận được theo hàm Horwitz. Trường hợp mẫu W-479 có giá trị RSD% cao hơn giá trị TRSD% dự báo có thể do sai số ngẫu nhiên của thiết bị đo hoặc cách lấy mẫu. Tuy nhiên, do nồng độ I- phân tích ở mức rất thấp (1 - 2mg/L) nên sai số phép đo đối với 1 trong tổng số 10 mẫu là có thể chấp nhận được.
Liên quan đến độ đúng của phương pháp, từ Bảng 5 có thể thấy có 8 trong tổng số 10 mẫu cho kết quả phân tích với độ lệch trong khoảng chấp nhận được (≤ 5%).
Mẫu W-463 có kết quả phân tích lệch nhiều so với kết quả đối chứng, nguyên nhân đến từ việc dung dịch gốc ban đầu có màu khá mạnh và điều này ảnh hưởng đến việc đo độ hấp thụ quang bằng phương pháp trắc quang so màu, dẫn đến sai lệch kết quả. Qua đây có thể thấy rõ yếu tố màu sắc của dung dịch gốc là trở ngại lớn đối với phương pháp phân tích trắc quang xác định I- trong nước vỉa.
4. Kết luận
Bài báo giới thiệu phương pháp nghiên cứu xác định nồng độ bromide và iodide trong nước vỉa bằng phân tích trắc quang được thực hiện dựa trên cơ sở phương pháp phân tích nước đã được chuẩn hóa trên thế giới. Giới hạn phát hiện 2 phương pháp đạt được là 0,1mg/L; độ tái lặp và độ đúng nằm trong phạm vi cho phép và đều nhỏ hơn 5% ở khoảng nồng độ phân tích thấp (< 200mg/L đối với Br- và < 5mg/L đối với I-) cho thấy việc áp dụng phương pháp này để xác định nồng độ Br-, I- trong nước vỉa là khả thi. Tuy nhiên, cần lưu ý phương pháp bị ảnh hưởng bởi màu dung dịch, độ đục và sự pha loãng mẫu. Nhằm hạn chế sai số phép đo cần loại bỏ hoặc giảm thiểu các yếu tố này bằng cách sử dụng máy pha loãng mẫu tự động cũng như khảo sát các hệ lọc thích hợp nhằm loại bỏ màu và độ đục của dung dịch mẫu gốc.
Tài liệu tham khảo
1. Hoàng Đình Tiến. Địa chất dầu khí và phương pháp tìm kiếm, thăm dò, theo dõi mỏ. Nhà xuất bản Đại học Quốc gia Tp. Hồ Chí Minh. 2006: trang 243 - 250.
2. Vũ Thu Hiền. Giáo trình thủy văn đại cương. Đại học Mỏ - Địa chất. 2010.
3. American Public Health Association (APHA), American Water Works Association (AWWA), Water Environment Federation (WEF). 4500-Br- B. Phenol red colorimetric method. Standard Methods for the Examination of Water and Wastewater (20th edition). 1999.
4. American Public Health Association (APHA), American Water Works Association (AWWA), Water Environment Federation (WEF). 4500-I- B. Leuco crystal violet method. Standard Methods for the Examination of Water and Wastewater (20th edition). 1999.