Tóm tắt
Bài báo giới thiệu kết quả nghiên cứu quá trình hòa tách xúc tác thải CuO-ZnO-Al2O3 của quá trình chuyển hóa CO nhiệt độ thấp bằng acid, sau đó tiến hành điện phân thu hồi Cu. Kết quả cho thấy quá trình hòa tách bằng acid sulfuric (H2SO4) nồng độ acid 1M, trong thời gian 3 giờ cho kết quả tốt tại nhiệt độ 50oC, tỷ lệ rắn/lỏng = 5%. Cu kim loại được thu hồi hoàn toàn bằng quá trình điện phân sau 7 giờ với điều kiện mật độ dòng 3,5A/dm2.
Từ khóa: Xúc tác thải chuyển hóa CO nhiệt độ thấp, hòa tách, H2SO4, HNO3, điện phân, thu hồi Cu.
1. Mở đầu
Lựa chọn công nghệ phù hợp để xử lý xúc tác thải rắn đang là vấn đề được nhiều nhà khoa học trong và ngoài nước quan tâm. Xúc tác thải cần phải được thu hồi và xử lý cẩn thận trước khi thải ra môi trường [1, 2]. Các nhà máy Đạm Phú Mỹ và Cà Mau, Lọc dầu Dung Quất đi vào hoạt động đã và đang thải ra một lượng xúc tác thải lớn, do vậy cần có các biện pháp xử lý thích hợp. Quá trình chuyển hóa CO nhiệt độ thấp là quá trình sử dụng trong nhà máy đạm nhằm chuyển hóa CO bằng hơi nước sử dụng hệ xúc tác CuO-ZnO-Al2O3 (xúc tác Nhà máy Đạm Phú Mỹ có thành phần: CuO 45 - 55%, ZnO 25 - 35%, Al2O3 5 - 15%, CuCO3 2 - 5%). Sau một thời gian làm việc, xúc tác bị mất hoạt tính do cốc che phủ bề mặt, bị ngộ độc bởi tạp chất hoặc bị chuyển pha. Xúc tác thải (sau 5 năm sử dụng) của quá trình này chứa một lượng CuO lớn không thể chôn lấp vì ảnh hưởng đến môi trường (CuO có thể gây độc với phổi, màng cơ, nếu tiếp xúc với CuO trong một thời gian dài có thể gây hại cho cơ thể người), vì vậy lượng Cu trong xúc tác thải cần được thu hồi, tái sử dụng.
Quá trình thu hồi kim loại từ xúc tác thải thường được tiến hành bằng quá trình hỏa luyện và thủy luyện. Quá trình thủy luyện thân thiện với môi trường hơn và chi phí thấp hơn nên chiếm ưu thế [3]. Tác nhân hòa tách có thể là dung dịch kiềm (ammoniac, điện lượng kế đồng để xác định hiệu suất dòng điện. Bộ nguồn điện 1 chiều có chức năng ổn định dòng được sử dụng trong khảo sát quá trình điện phân.
Hiệu suất dòng được tính theo công thức: muối amoni, NaOH, Na2CO3…), acid vô cơ (sulfuric, nitric và hydrochloric acid…) hoặc acid hữu cơ (tartaric, oxalic và citric acid…) [1]. Quá trình hòa tách để thu kim loại từ xúc tác thải bằng acid vô cơ là quá trình hay được sử dụng nhất [4]. Trước khi tiến hành hòa tách, xúc tác thải thường được xử lý nhiệt để loại bỏ cốc, hydrocarbon và một số tạp chất khác, nhằm tăng cường hiệu quả hòa tách [5].
Việc nghiên cứu công nghệ thu hồi kim loại từ xúc tác thải rắn vừa có ý nghĩa lý thuyết vừa có ý nghĩa thực tế, góp phần bảo vệ môi trường và thu hồi kim loại từ chất thải rắn. Trong nước đã có một số công trình nghiên cứu quá trình xử lý, tái sử dụng xúc tác thải của nhà máy lọc dầu và thu hồi Ni từ nhà máy đạm [6]. Quá trình thu hồi Cu từ xúc tác thải của nhà máy đạm chưa được nghiên cứu. Bài báo trình bày kết quả nghiên cứu công nghệ thủy luyện (hòa tan xúc tác thải CuO-ZnO-Al2O3 của quá trình chuyển hóa CO nhiệt độ thấp trong acid), sau đó tiến hành điện phân thu hồi Cu. Đây là một trong những công nghệ có tính khả thi cao: vừa tiết kiệm năng lượng, vừa bảo vệ môi trường.
2. Thực nghiệm
Xúc tác trước khi hòa tách được nghiền tới kích thước 0,5mm, nung ở 800oC trong 3 giờ. Quá trình hòa tách xúc tác thải chứa Cu được thực hiện với acid sulfuric và acid nitric nồng độ 0,5 - 2M, từ nhiệt độ phòng đến 90oC, trong khoảng thời gian 1 - 3 giờ và tỷ lệ rắn/lỏng: 3 - 6%. Dung dịch hòa tách thu được sau khi lọc được đem điện phân. Mật độ dòng giới hạn của quá trình điện phân được xác định trên máy đo điện hóa Potentiostat/Galvanostat (Autolab PGSTAT 302N). Quá trình khảo sát đường cong điện hóa được thực hiện trong bình đo điện hóa ba điện cực với điện cực đối platin, điện cực làm việc bằng đồng và điện cực so sánh calomen. Trong quá trình nghiên cứu điện phân, điện cực anode được chế tạo từ thép không gỉ, cathode bằng đồng, mạch điện phân có mắc thêm điện lượng kế đồng để xác định hiệu suất dòng điện. Bộ nguồn điện 1 chiều có chức năng ổn định dòng được sử dụng trong khảo sát quá trình điện phân.
Hiệu suất dòng được tính theo công thức:
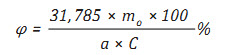
Trong đó:
mo: Khối lượng đồng kết tủa trên cathode dung dịch điện phân (g);
a: Khối lượng đồng kết tủa trên cathode dung dịch điện lượng kế (g);
C: Trọng lượng đương lượng của kim loại làm cathode = 31.785.
Hiệu suất thu hồi được tính theo công thức:
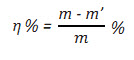
Trong đó:
m: Hàm lượng đồng trong dung dịch ban đầu (g/l);
m’: Hàm lượng đồng trong dung dịch sau điện phân (g/l).
Hàm lượng đồng trong dung dịch được xác định bằng UV-Vis tại bước sóng 805nm [7]. Xúc tác thải và phần bã còn lại phân tích đặc trưng bằng phương pháp XRD (thực hiện trên máy D8 Advance - Bruker) và FESEM (thực hiện trên máy Hitachi S4800) được kết nối với EDX (trên máy JEOL - JED 2300).
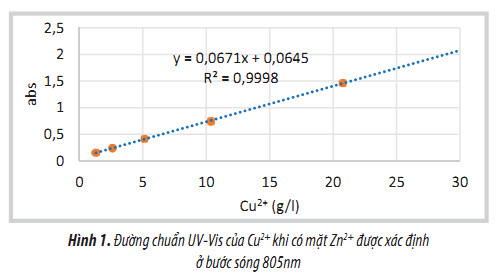
Đường chuẩn UV-Vis của Cu2+ khi có mặt Zn2+ được thể hiện trên Hình 1.
3. Kết quả và thảo luận
3.1. Đặc trưng xúc tác thải trước và sau khi nung
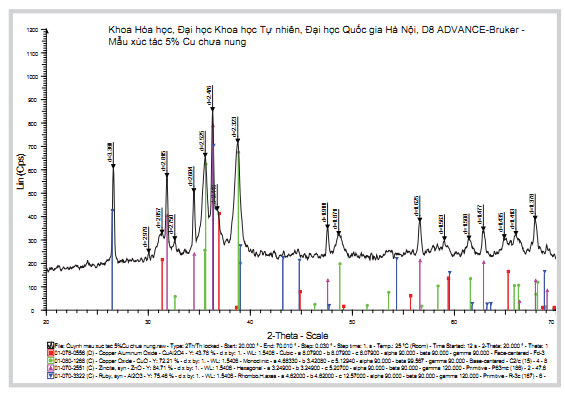
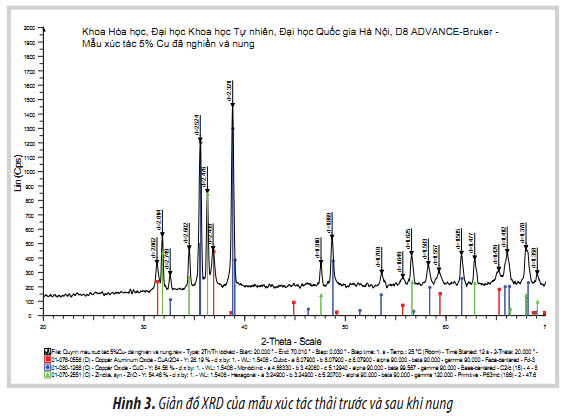
Xúc tác thải lấy từ Nhà máy Đạm Phú Mỹ trước và sau khi nung được tiến hành chụp ảnh SEM, phân tích thành phần hóa học bằng EDX và thành phần pha bằng XRD. Kết quả được trình bày trong Hình 2, 3 và Bảng 1.
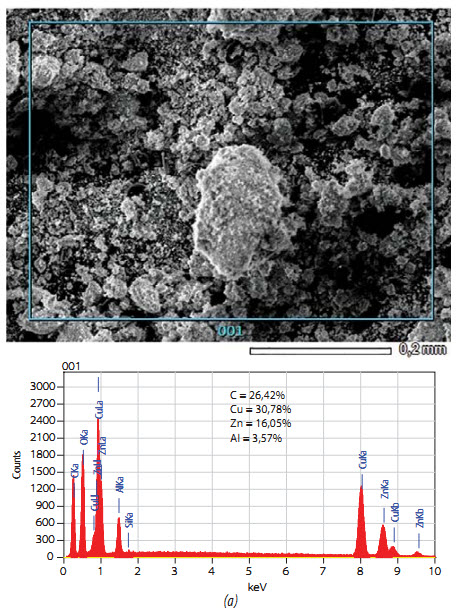
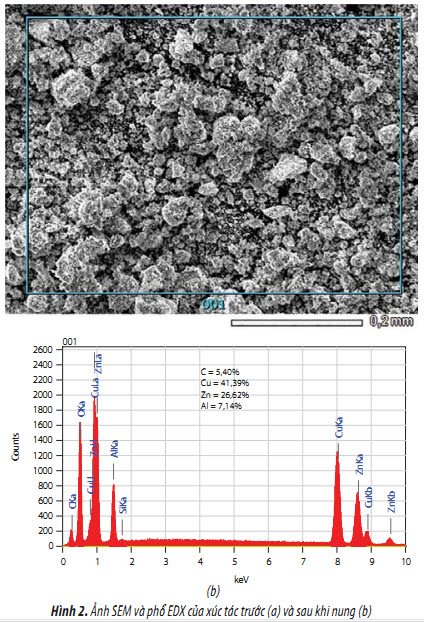
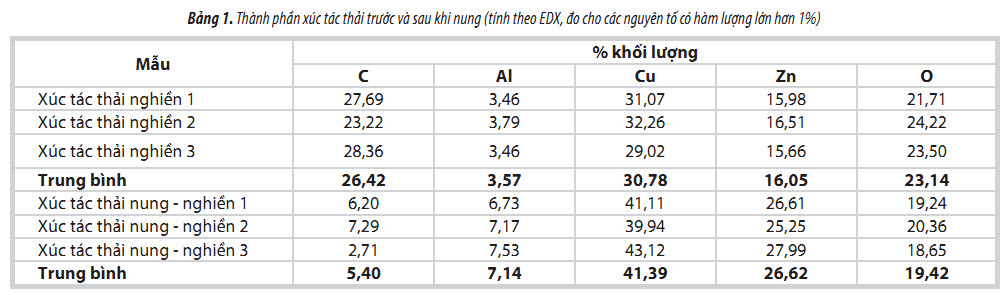
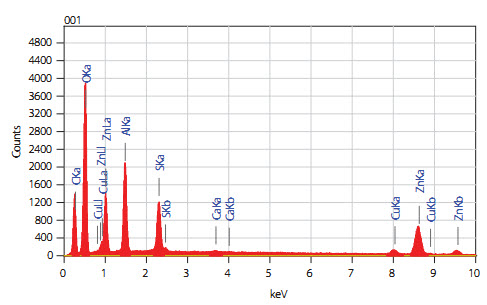
Ảnh SEM cho thấy xúc tác thải bị thiêu kết và có một lượng lớn cốc bám trên bề mặt, đây là những nguyên nhân quan trọng nhất gây mất hoạt tính xúc tác. Hàm lượng C tính theo EDX là 26,42%. Để tăng khả năng khuếch tán của acid vào phía trong hạt xúc tác, cần loại bỏ cốc bằng cách nung. Sau khi nung hàm lượng C giảm xuống còn 5,4% (Bảng 1).
Giản đồ XRD cho thấy ngoài 3 thành phần CuO-ZnO-Al2O3, trong xúc tác thải còn tồn tại pha CuAl2O4. Như vậy, ngoài nguyên nhân mất hoạt tính do tạo cốc, một nguyên nhân mất hoạt tính khác có thể kể đến là sự tương tác của CuO với Al2O3 để tạo thành CuAl2O4. Sau khi nung, pha Al2O3 trong xúc tác thải không còn, có thể ở nhiệt độ cao pha này đã bị chuyển sang dạng CuAl2O4 theo phản ứng:
CuO + Al2O3 → CuAl2O4
3.2. Nghiên cứu quá trình hòa tách bằng acid
3.2.1. Nghiên cứu ảnh hưởng của nồng độ acid
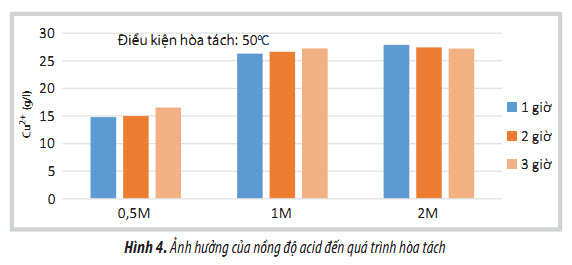
Nhóm tác giả đã nghiên cứu quá trình hòa tách bằng acid sulfuric với nồng độ acid thay đổi từ 0,5 - 1 - 2M, điều kiện hòa tách ở nhiệt độ 50oC. Kết quả cho thấy, khi tăng nồng độ acid từ 0,5 đến 1M, độ hòa tách tăng lên đáng kể, tiếp tục tăng nồng độ acid lên 2M độ hòa tách hầu như không tăng, vì vậy nồng độ acid 1M được lựa chọn cho các nghiên cứu tiếp theo (Hình 4).
3.2.2. Nghiên cứu ảnh hưởng của tỷ lệ rắn/lỏng
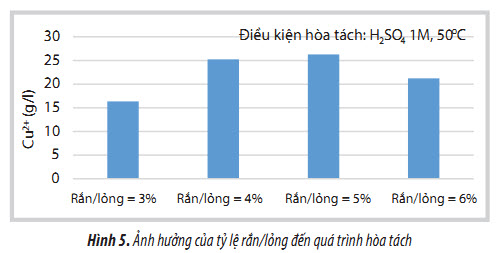
Ảnh hưởng của tỷ lệ rắn/lỏng được trình bày trong Hình 5. Điều kiện hòa tách ở nhiệt độ 50oC, nồng độ H2SO4 1M, tỷ lệ rắn/lỏng từ 3 đến 6%. Tỷ lệ rắn/lỏng thấp, lượng xúc tác thải ít nên lượng Cu thu hồi được thấp. Khi tăng tỷ lệ rắn/ lỏng lên 6%, lượng Cu thu được giảm, điều này có thể giải thích do ở tỷ lệ này lượng chất rắn tăng làm tăng mật độ rắn trong dung dịch dẫn tới giảm khả năng tiếp xúc giữa xúc tác thải và dung dịch hòa tách do vậy làm giảm hiệu quả hòa tách. Kết quả cho thấy ở tỷ lệ rắn/lỏng = 5%, lượng Cu thu được cao nhất.
3.2.3. Nghiên cứu ảnh hưởng của loại acid
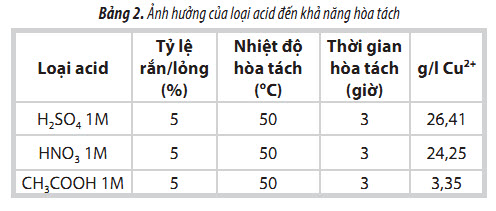
Tiến hành hòa tách trong cùng điều kiện tỷ lệ rắn/ lỏng, nhiệt độ, thời gian hòa tách, sử dụng các acid khác nhau. Kết quả trình bày trong Bảng 2. Trong 3 loại acid sử dụng, acid sulfuric cho hiệu quả tách tốt nhất. Acid acetic hầu như không hòa tách được Cu ở nhiệtđộ thấp.
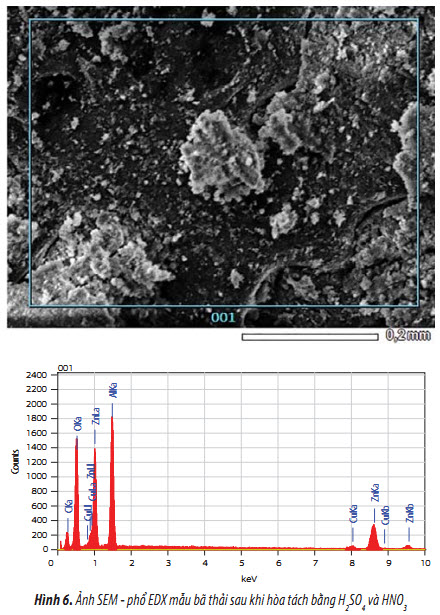
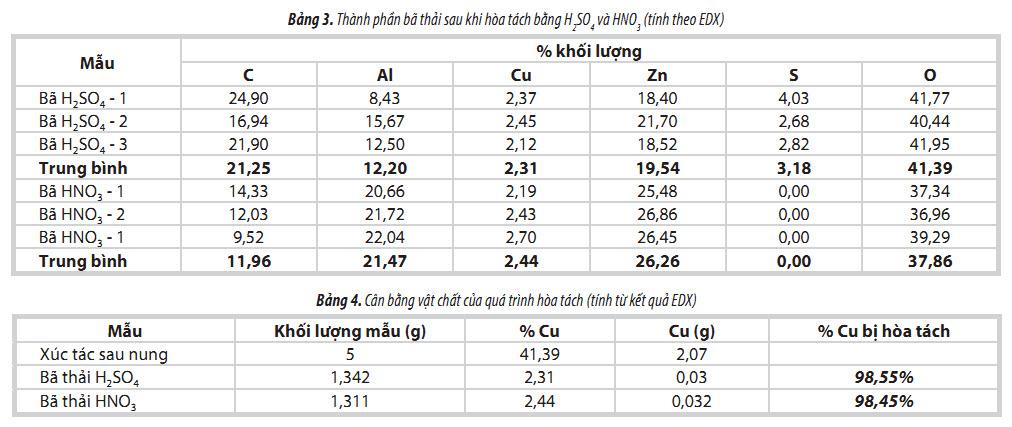
Phần bã thải rắn sau hòa tách được phân tích bằng SEM-EDX, kết quả được trình bày trong Hình 6 và Bảng 3.
Sau khi hòa tách hàm lượng Cu trong bã thải giảm đi đáng kể, lượng Cu còn lại là 2,31 - 2,44%. Cân bằng vật chất của quá trình hòa tách (xác định theo EDX) được trình bày trong Bảng 4.
Như vậy quá trình hòa tách đã tách được > 98% lượng Cu trong mẫu xúc tác thải.
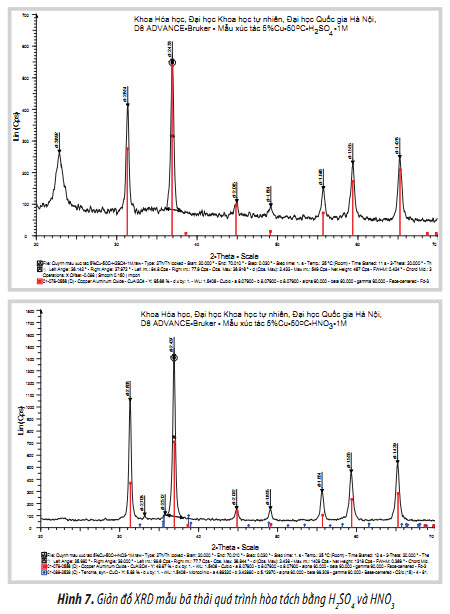
Giản đồ XRD của mẫu bã thải sau quá trình hòa tách được trình bày trong Hình 7.
Sau quá trình hòa tách, các pha CuO và ZnO không còn, chứng tỏ CuO và ZnO đã bị hòa tan hết, mẫu bã thải chỉ còn tồn tại pha CuAl2O4, đây là pha tương đối bền. Kết quả này cũng phù hợp với kết quả phân tích EDX (hàm lượng Cu trong bã thải vẫn còn 2,31 - 2,44%).

3.2.4. Nghiên cứu ảnh hưởng của nhiệt độ và thời gian hòa tách
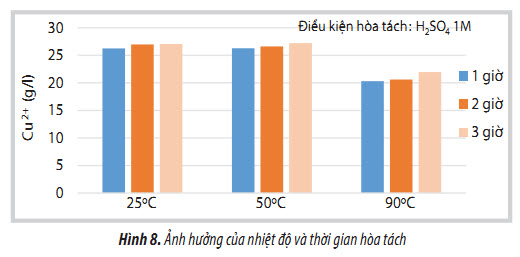
Ảnh hưởng của nhiệt độ và thời gian hòa tách được trình bày trong Hình 8.
Thời gian hòa tách tăng, lượng đồng thu được cũng tăng nhưng không nhiều. Ở nhiệt độ thấp dưới 200 50oC, quá trình hòa tách không bị ảnh hưởng nhiều bởi nhiệt độ, tuy nhiên khi tăng nhiệt độ lên 90oC quá trình hòa tách giảm. Kết quả tương tự cũng được I.M.Ahmed và cộng sự công bố [8]. Điều này có thể giải thích do ở nhiệt độ cao, Zn bị hòa tan sẽ bị polymer hóa và thủy phân, làm giảm hiệu quả quá trình hòa tách. Quá trình hòa tách ở nhiệt độ 25oC cho hiệu quả thu hồi Cu tương tự như ở 50oC, nhưng độ nhớt của dung dịch cao hơn, làm quá trình khuấy trộn khó hơn. Khi tiến hành trong phòng thí nghiệm ở lượng nhỏ, ảnh hưởng của độ nhớt không lớn, tuy nhiên, nếu tiến hành ở quy mô lớn hơn, độ nhớt sẽ ảnh hưởng đáng kể, vì vậy nhiệt độ 50oC vẫn được chọn là nhiệt độ thích hợp cho quá trình hòa tách.
3.3. Nghiên cứu điện phân thu hồi Cu từ dung dịch đã hòa tách
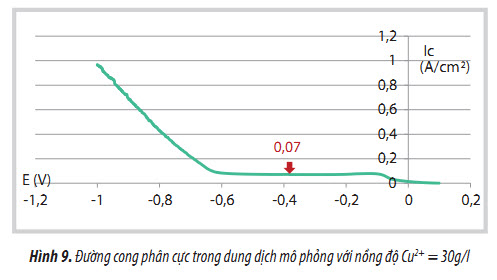
3.3.1. Xác định mật độ dòng tới hạn với dung dịch mô phỏng
Để tìm được mật độ dòng điện hợp lý trong quá trình điện phân nhóm tác giả tiến hành đo đường cong phân cực của các mẫu trước khi tiến hành điện phân. Từ đường cong phân cực nhận thấy mật độ dòng tới hạn đối với dung dịch hòa tách là 0,07A/cm2 hay 7A/ dm2. Vì vậy, để đảm bảo hiệu suất cao cho quá trình điện phân thu hồi đồng, quá trình điện phân dung dịch hòa tách xúc tác thải được tiến hành với mật độ dòng ≤ 3,5A/dm2.
3.3.2. Nghiên cứu ảnh hưởng của mật độ dòng tới khả năng thu hồi Cu từ dung dịch đã hòa tách
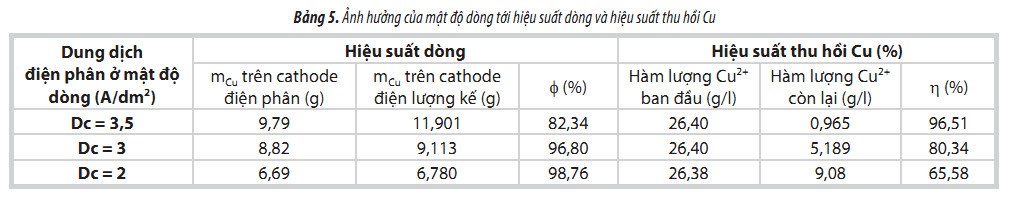
Tiến hành quá trình điện phân ở mật độ dòng 2 - 3 và 3,5A/dm2 tại nhiệt độ phòng, kết quả thu được sau 6 giờ điện phân được trình bày trong Bảng 5.
Khi mật độ dòng điện áp đặt vào bình điện phân tăng, lượng đồng thu hồi tăng lên đáng kể, thể hiện qua việc tăng hiệu suất thu hồi đồng (η), điều này phù hợp với định luật Faraday của quá trình điện phân. Khi mật độ dòng điện phân tăng, điện lượng qua mạch sẽ tăng lên. Do đó, lượng đồng kết tủa lên điện cực cathode tỷ lệ thuận với điện lượng qua mạch, sẽ tăng lên cùng với việc tăng dòng điện phân. Tuy nhiên, khi tăng mật độ dòng điện phân, hiệu suất dòng sẽ giảm do trong cùng một khoảng thời gian điện phân, khi điện phân ở mật độ dòng cao, lượng ion đồng sẽ giảm nhanh, dẫn đến mật độ dòng giới hạn của quá trình điện phân sẽ giảm, quá trình giải phóng hydro có thể diễn ra làm giảm hiệu suất dòng điện phân đồng.
3.3.3. Nghiên cứu ảnh hưởng của thời gian điện phân
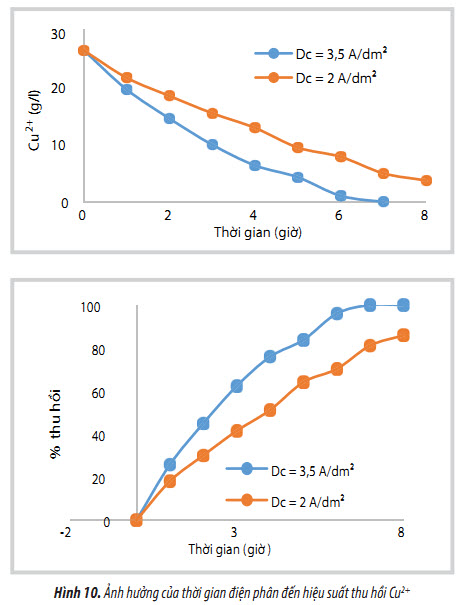
Ảnh hưởng của thời gian điện phân đến khả năng thu hồi đồng từ dung dịch hòa tách xúc tác thải được trình bày trong Hình 10 và 11.
Hiệu suất thu hồi của các mẫu điện phân tăng dần theo thời gian. Theo định luật Faraday, lượng kim loại kết tủa ở điện cực cathode tỷ lệ thuận với lượng điện tích qua mạch, do đó tỷ lệ thuận với thời gian điện phân. Ở mật độ dòng 3,5A/dm2, sau khoảng thời gian 7 giờ điện phân hiệu suất thu hồi đồng đạt cao nhất (~ 100%).

Kết luận
- Nhóm tác giả đã nghiên cứu quá trình hòa tách xúc tác thải của quá trình chuyển hóa CO ở nhiệt độ thấp của Nhà máy Đạm Phú Mỹ bằng acid sulfuric, sau đó điện phân thu hồi đồng.
- Các điều kiện thích hợp cho quá trình hòa tách là H2SO4 nồng độ acid 1M, trong thời gian 3 giờ tại 50oC, tỷ lệ rắn/lỏng = 5%, hàm lượng Cu2+ thu được đạt 26,41g/l.
- Quá trình điện phân với mật độ dòng càng cao thì hiệu suất dòng càng giảm và hiệu suất thu hồi đồng càng cao. Sau 7 giờ điện phân tại mật độ dòng 3,5A/dm2 hiệu suất thu hồi đồng đạt ~ 100%.
- Các kết quả nghiên cứu cho thấy có thể hòa tách trên 98% lượng Cu trong xúc tác thải và thu hồi gần 100% lượng Cu trong dung dịch đã hòa tách. Đây là quá trình có triển vọng, tuy nhiên để có thể áp dụng trong công nghiệp cần tiếp tục nghiên cứu tái sử dụng acid sau khi điện phân.
Lời cảm ơn
Công trình được thực hiện với sự hỗ trợ kinh phí của đề tài “UK Institutional Links (Ref 172711746)”. Cảm ơn Nhà máy Đạm Phú Mỹ đã cung cấp xúc tác thải cho đề tài.
Tài liệu tham khảo
1. M.Marafi, A.Stanislaus. Spent hydroprocessing catalyst management: A review. Part II. Advances in metal recovery and safe disposal methods. Resources, Conservation and Recycling. 2008; 53(1 - 2): p. 1 - 26.
2. P.K.Parhi, T.R.Sethy, P.C.Rout, K.Sarangi. Selective dissolution of copper from copper-chromium spent catalyst by baking-leaching process. Journal of Industrial and Engineering Chemistry. 2015; 21: p. 604 - 609.
3. V.S.Kolosnitsyn, S.P.Kosternova, O.A.Yapryntseva, A.A.Ivashchenko, S.V.Alekseev. Recovery of nickel with sulfuric acid solutions from spent catalysts for steam conversion of methane. Russian Journal of Applied Chemistry. 2006; 79(4): p. 539 - 543.
4. A.R.Sheik, M.K.Ghosh, K.Sanjay, T.Subbaiah, B.K.Mishra, A.A.Baba. Aqueous processing of nickel spent catalyst for a value added product. Korean Journal of Chemical. Engineering. 2013; 30(2): p. 400 - 404.
5. S.P.Barik, K.H.Park, P.K.Parhi, J.T. Park, C.W.Nam. Extraction of metal values from waste spent petroleum catalyst using acidic solutions. Separation and Purification Technology. 2012; 101: p. 85 - 90.
6. Lê Phúc Nguyên, Bùi Vĩnh Tường, Nguyễn Hoài Thu, Nguyễn Sura, Lương Ngọc Thủy. Thu hồi Ni trong xúc tác thải để tổng hợp xúc tác xử lý môi trường: Nghiên cứu ảnh hưởng của điều kiện tiền xử lý và ảnh hưởng của hàm lượng Ni trong xúc tác Ni/γ-Al2O3 đến khả năng xử lý CO. Tạp chí Dầu khí. 2015; 1: trang 42 - 51.
7. S.Silva-Martinez, S.Roy. Copper recovery from tin stripping solution: Galvanostatic deposition in a batch-recy- cle system. Separation and Purification Technology. 2013; 118: p. 6 - 12.
8. I.M.Ahmed, A.A.Nayl, J.A.Daoud. Leaching and recovery of zinc and copper from brass slag by sulfuric acid. Journal of Saudi Chemical Society. 2012.
Recovery of copper from spent catalyst of low temperature water gas shift from Phu My fertilizer plant
Ngo Thuy Quynh - Hanoi University of Science and Technology - Ministry of Industry and Trade, Nguyen Thi Thu Huyen - Hanoi University of Science and Technology
Nguyen Thi Kim Anh - Hanoi University of Science and Technology, Nguyen Thi Phuong - Hanoi University of Science and Technology
Dang Trung Dung - Hanoi University of Science and Technology, Mai Thanh Tung - Hanoi University of Science and Technology
Pham Thanh Huyen - Hanoi University of Science and Technology, Sudipta Roy - University of Strathclyde, Glasgow, UK
Email: huyen.phamthanh@hust.edu.vn
Summary
The paper presents the results of leaching CuO-ZnO-Al2O3 spent catalyst of low temperature water gas shift by acid and then electrodepositing the leaching solution to recover copper. It was found that the suitable conditions for copper leaching from low temperature water gas shift’s spent catalyst are at 50oC with 1M H2SO4 and solid/liquid ratio of 5%. Copper was totally recovered after 7 hours with a current density of 3.5A/dm2.
Key words: Low temperature water gas shift’s spent catalyst, leaching, H2SO4, HNO3, electrolysis, copper recovery.